Гальваническое покрытие - это процесс покрытия одного металла другим при помощи осаждения его из водных растворов солей под действием электрического тока. Покрываемые изделия служат катодами, анодом - вспомогательный электрод, подключенный к положительному полюсу источника тока.
Гальваническая ванна состоит из электролита и погруженных в нее электродов, через которые проходит электрический ток от металлического проводника к электролиту (рис.2.1). Если через раствор (электролит) пропустить ток. то положительно заряженные ионы металла будут двигаться к катод) (отрицательно заряженному электроду) и осаждаться на нем. Отрицательно заряженные ионы к аноду (положительно заряженный электрод). В гальванической ванне обычно катодом служат изделия. а анодом - металл, которым необходимо покрыть изделия.
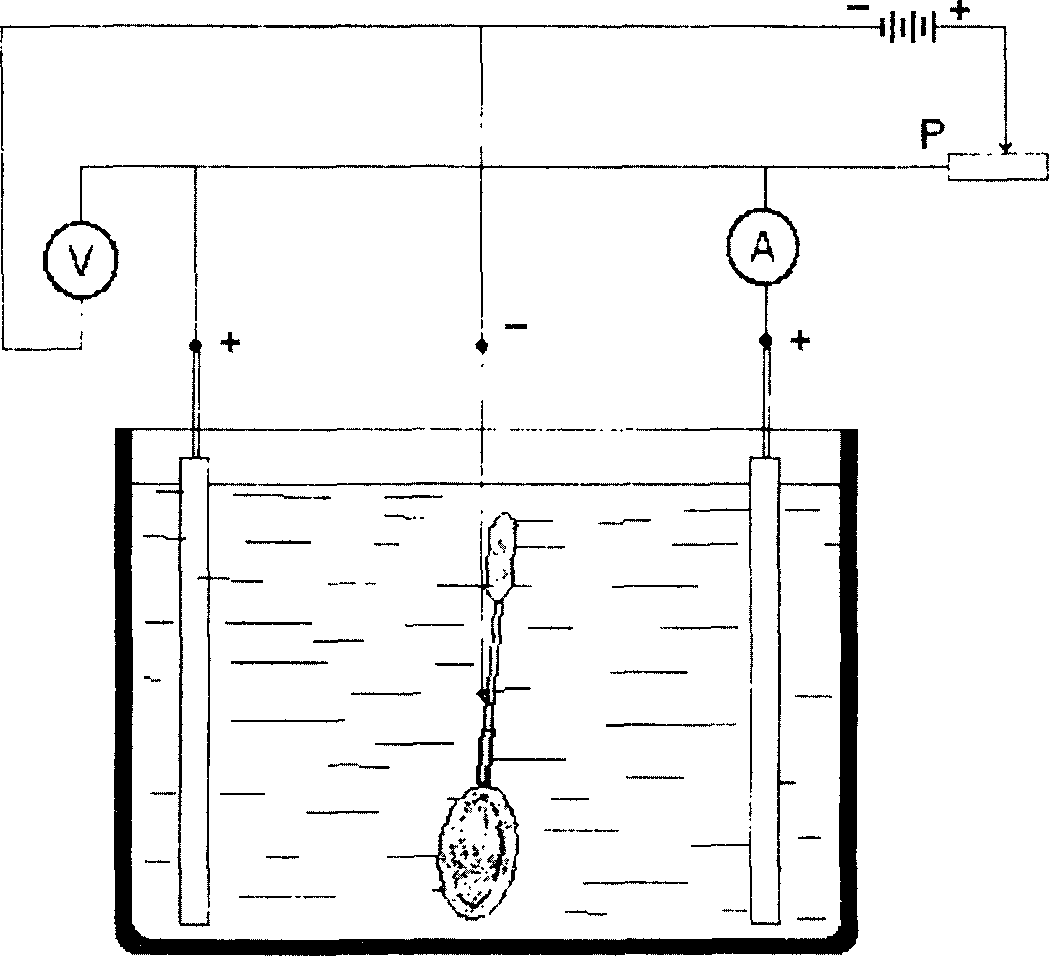 |
Рис.2.1. Схема гальванической ванны: Р - реостат; Л - амперметр: V вольтметр; г ■ анод: - -- катод (изделие) |
2.1. Процесс осаждения металла из электролитов.
Принцип работы гальванической ванны с растворимыми анодами заключается в отдаче ионов металла (анода) в раствор по уравнению.
Me —> Vie" ь пе.
Нерастворимый анод не передает в электролит никаких ионов, т. е. при анодной реакции окисления анод не растворяется. На нерастворимых анодах происходит анодное выделение кислорода. В щелочных электролитах выделение кислорода проходит по уравнению.
40Н" --* 2Н
0 + О:
4е,.
в кислых электролитах - по уравнению:.
4Н;0 --» 4Н"~ О; - 4е.
Анодные реакции окисления на нерастворимых анодах могут привести к изменению состава электролита, которое имеет большое значение для работы ванн.
